Como se mide el radio atomico en la tabla periodica
La tabla periódica es una herramienta fundamental en la química. En ella podemos encontrar información vital sobre los elementos químicos, como su número atómico, su símbolo, su masa atómica, su configuración electrónica, su estado de oxidación y, por supuesto, su radio atómico.
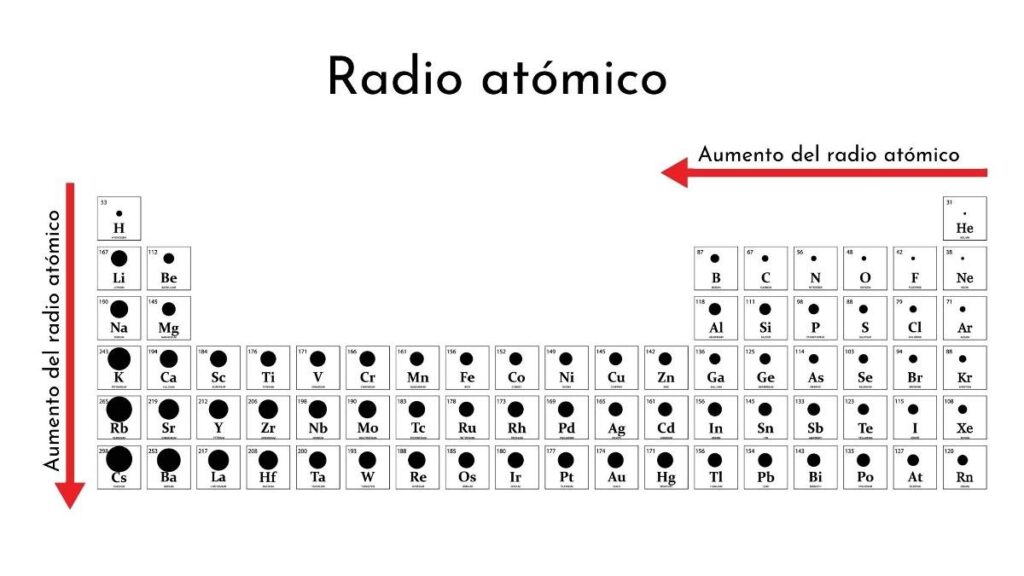
El radio atómico es una propiedad periódica que se refiere al tamaño del átomo. En general, el radio atómico disminuye a medida que nos movemos hacia la derecha en la tabla periódica y aumenta a medida que nos movemos hacia abajo. Esto se debe a la forma en que están dispuestos los electrones en los átomos.
Existen varios métodos para medir el radio atómico, pero uno de los más comunes es el método de difracción de rayos X. En este método, se irradia un cristal con rayos X y se miden los ángulos y las intensidades de los rayos difractados. A partir de esta información, se pueden calcular las distancias entre los átomos en el cristal y, por lo tanto, el radio atómico.
Otro método común para medir el radio atómico es la espectroscopía de emisión atómica. En este método, se excita un átomo mediante una fuente de energía, como un arco eléctrico, y se mide la longitud de onda de la luz emitida por el átomo. A partir de esta información, se puede determinar el tamaño del átomo.
También existen métodos teóricos para calcular el radio atómico, como la teoría de la densidad electrónica. En esta teoría, se calcula la densidad de electrones alrededor del núcleo del átomo y se utiliza esta información para determinar el tamaño del átomo.
En resumen, El radio atómico es una propiedad importante de los elementos químicos que se puede medir de varias maneras, como la difracción de rayos X, la espectroscopía de emisión atómica y la teoría de la densidad electrónica. Comprender el radio atómico es crucial para comprender las propiedades y el comportamiento de los elementos en la tabla periódica.
Comparación de radios atómicos
Una forma útil de entender el radio atómico es comparar los radios de diferentes elementos en la tabla periódica. A continuación, se muestra una tabla que compara los radios atómicos de los elementos en el tercer período de la tabla periódica.
| Elemento | Radio atómico (pm) |
|---|---|
| Sodio (Na) | 186 |
| Magnesio (Mg) | 160 |
| Aluminio (Al) | 143 |
| Silicio (Si) | 117 |
| Fósforo (P) | 110 |
| Azufre (S) | 104 |
| Cloro (Cl) | 99 |
Como se puede observar, el radio atómico disminuye a medida que se avanza hacia la derecha de la tabla periódica. Esto se debe a que a medida que se agregan electrones a la capa exterior de un átomo, la carga nuclear efectiva aumenta, lo que atrae más fuertemente a los electrones y hace que el átomo sea más pequeño.
Del mismo modo, el radio atómico aumenta a medida que se avanza hacia abajo en la tabla periódica. Esto se debe a que a medida que se mueve hacia abajo en un grupo, se agrega una capa de electrones a la capa exterior del átomo, lo que aumenta el tamaño del átomo.
Factores que afectan el radio atómico
Además de la posición de un elemento en la tabla periódica, hay otros factores que pueden afectar el radio atómico. Algunos de estos factores incluyen:
Carga nuclear efectiva
La carga nuclear efectiva se refiere a la fuerza con la que el núcleo de un átomo atrae a los electrones de la capa exterior. A medida que la carga nuclear efectiva aumenta, el radio atómico disminuye. Esto se debe a que los electrones de la capa exterior son atraídos más fuertemente hacia el núcleo, lo que hace que el átomo sea más pequeño.
Número de electrones en la capa exterior
El número de electrones en la capa exterior de un átomo también puede afectar el radio atómico. A medida que se agrega un electrón a la capa exterior de un átomo, el radio atómico disminuye. Esto se debe a que la carga nuclear efectiva aumenta, lo que atrae más fuertemente a los electrones y hace que el átomo sea más pequeño.
Estado de oxidación
El estado de oxidación se refiere al número de electrones que un átomo ha perdido o ganado en una reacción química. A medida que un átomo pierde electrones, su carga nuclear efectiva aumenta, lo que hace que su radio atómico disminuya. Del mismo modo, a medida que un átomo gana electrones, su carga nuclear efectiva disminuye y su radio atómico aumenta.
Preguntas frecuentes sobre el radio atómico
¿Por qué el radio atómico disminuye a medida que se mueve hacia la derecha en la tabla periódica?
El radio atómico disminuye a medida que se mueve hacia la derecha en la tabla periódica debido a la carga nuclear efectiva. A medida que se agregan electrones a la capa exterior de un átomo, la carga nuclear efectiva aumenta, lo que atrae más fuertemente a los electrones y hace que el átomo sea más pequeño.
¿Por qué el radio atómico aumenta a medida que se mueve hacia abajo en la tabla periódica?
El radio atómico aumenta a medida que se mueve hacia abajo en la tabla periódica debido al número de capas de electrones. A medida que se mueve hacia abajo en un grupo, se agrega una capa de electrones a la capa exterior del átomo, lo que aumenta el tamaño del átomo.
¿Cómo se mide el radio atómico?
El radio atómico se puede medir de varias maneras, como la difracción de rayos X, la espectroscopía de emisión atómica y la teoría de la densidad electrónica.
¿Qué factores afectan el radio atómico?
El radio atómico puede ser afectado por la carga nuclear efectiva, el número

Deja una respuesta