Cuales son las moleculas que se presentan en los reactivos
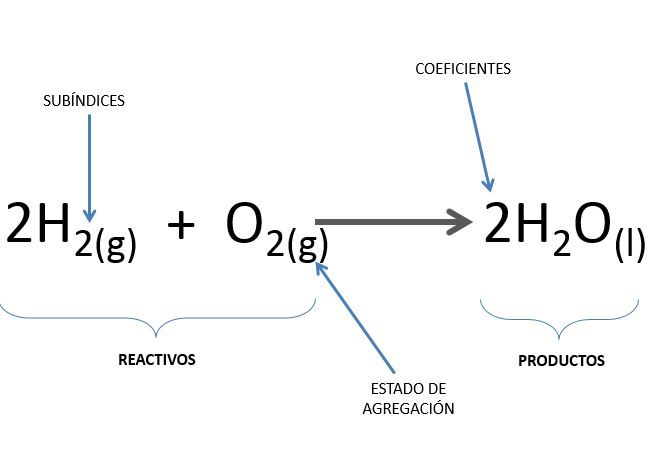
La química es una ciencia fascinante que estudia la composición, estructura, propiedades y transformaciones de la materia. Los reactivos son sustancias químicas que se utilizan para llevar a cabo una reacción química, y para que se produzca una reacción química es necesario que los reactivos interactúen entre sí. En este artículo, exploraremos las moléculas que se presentan en los reactivos y cómo interactúan entre sí.
¿Qué son las moléculas?
Para entender las moléculas que se presentan en los reactivos, es importante saber qué son las moléculas. Las moléculas son la unidad básica de la materia, que consisten en dos o más átomos unidos por enlaces químicos. Las moléculas pueden ser simples, como la molécula de agua (H2O), o complejas, como la molécula de proteína.
Reactivos y moléculas
Los reactivos son sustancias químicas que se utilizan para llevar a cabo una reacción química. Las moléculas que se presentan en los reactivos pueden ser simples o complejas, y se combinan entre sí para producir una nueva sustancia. En una reacción química, los reactivos se transforman en productos, y la cantidad de reactivos y productos se mantiene constante.
Moléculas en reacciones de ácido-base
En una reacción de ácido-base, los reactivos son un ácido y una base. Los ácidos son sustancias que liberan iones de hidrógeno (H+) en solución acuosa, mientras que las bases son sustancias que liberan iones hidroxilo (OH-) en solución acuosa. En esta reacción, los iones H+ y OH- se combinan para formar agua (H2O). Por ejemplo, en la reacción de ácido clorhídrico (HCl) y hidróxido de sodio (NaOH), los reactivos son HCl y NaOH, y los productos son agua (H2O) y cloruro de sodio (NaCl).
Moléculas en reacciones de oxidación-reducción
En una reacción de oxidación-reducción, los reactivos son un oxidante y un reductor. Un oxidante es una sustancia que acepta electrones, mientras que un reductor es una sustancia que dona electrones. En esta reacción, los electrones se transfieren de un reactivo a otro para producir un producto. Por ejemplo, en la reacción de hierro (Fe) y oxígeno (O2), los reactivos son Fe y O2, y el producto es óxido de hierro (Fe2O3).
Moléculas en reacciones de precipitación
En una reacción de precipitación, los reactivos son dos soluciones que contienen iones que reaccionan para producir un sólido insoluble. Por ejemplo, en la reacción de nitrato de plata (AgNO3) y cloruro de sodio (NaCl), los reactivos son AgNO3 y NaCl, y el producto es cloruro de plata (AgCl), que es un sólido insoluble en agua.
Conclusión
En resumen, Las moléculas que se presentan en los reactivos pueden ser simples o complejas, y se combinan entre sí para producir una nueva sustancia en una reacción química. En una reacción de ácido-base, los reactivos son un ácido y una base, mientras que en una reacción de oxidación-reducción, los reactivos son un oxidante y un reductor. En una reacción de precipitación, los reactivos son dos soluciones que contienen iones que reaccionan para producir un sólido insoluble.
Preguntas frecuentes
1. ¿Qué son los reactivos en química?
Los reactivos son sustancias químicas que se utilizan para llevar a cabo una reacción química.
2. ¿Qué son las moléculas?
Las moléculas son la unidad básica de la materia, que consisten en dos o más átomos unidos por enlaces químicos.
3. ¿Qué es una reacción de ácido-base?
En una reacción de ácido-base, los reactivos son un ácido y una base. Los ácidos son sustancias que liberan iones de hidrógeno (H+) en solución acuosa, mientras que las bases son sustancias que liberan iones hidroxilo (OH-) en solución acuosa.
4. ¿Qué es una reacción de oxidación-reducción?
En una reacción de oxidación-reducción, los reactivos son un oxidante y un reductor. Un oxidante es una sustancia que acepta electrones, mientras que un reductor es una sustancia que dona electrones.
5. ¿Qué es una reacción de precipitación?
En una reacción de precipitación, los reactivos son dos soluciones que contienen iones que reaccionan para producir un sólido insoluble.

Deja una respuesta