Ejemplos de la ley de la conservacion de la materia
La ley de la conservación de la materia es una regla fundamental de la química que establece que la materia no puede ser creada ni destruida, solo transformada. En otras palabras, la cantidad total de materia en un sistema cerrado permanece constante a lo largo del tiempo. Esta ley es una de las más importantes en la química y se aplica en una amplia gama de situaciones. A continuación, se presentan algunos ejemplos de la ley de la conservación de la materia.
- 1. Combustión
- 2. Fotosíntesis
- 3. Reacciones químicas
- 4. Cambios de fase
- Conclusión
- Preguntas frecuentes
- 1. ¿Por qué es importante la ley de la conservación de la materia?
- 2. ¿Cómo se relaciona la ley de la conservación de la materia con la energía?
- 3. ¿Qué es un sistema cerrado?
- 4. ¿Cómo se aplica la ley de la conservación de la materia en la vida cotidiana?
- 5. ¿Cuál es la relación entre la ley de la conservación de la materia y la ley de la conservación de la masa?
1. Combustión
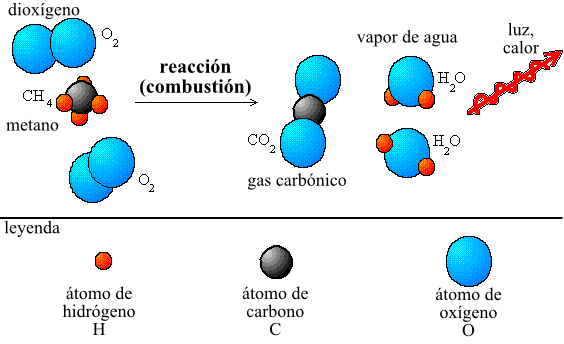
Cuando se quema un trozo de madera, la madera se convierte en ceniza y gases como el dióxido de carbono y el vapor de agua. Si se pesa la madera antes y después de quemarla, se encontrará que la masa total es la misma. Esto se debe a que los átomos de carbono e hidrógeno en la madera se combinan con el oxígeno del aire para formar los gases de la combustión. Aunque la madera se haya transformado en ceniza y gases, la cantidad total de materia en el sistema sigue siendo la misma.
2. Fotosíntesis
La fotosíntesis es el proceso mediante el cual las plantas convierten la energía solar en energía química para almacenarla como azúcares. Durante este proceso, el dióxido de carbono del aire y el agua se combinan para formar glucosa y oxígeno. Aunque la masa total de la planta aumenta a medida que crece, la cantidad total de materia en el sistema sigue siendo la misma. Esto se debe a que la materia no se crea ni se destruye durante la fotosíntesis, solo se transforma.
3. Reacciones químicas
Las reacciones químicas también están sujetas a la ley de la conservación de la materia. Por ejemplo, cuando se mezcla ácido clorhídrico y hidróxido de sodio, se produce cloruro de sodio (sal común) y agua. Aunque los reactivos y los productos tienen diferentes propiedades químicas y físicas, la cantidad total de materia en el sistema sigue siendo la misma.
4. Cambios de fase
Los cambios de fase, como la fusión y la evaporación, también están sujetos a la ley de la conservación de la materia. Cuando se derrite un cubo de hielo, el agua se transforma de sólido a líquido, pero la cantidad total de materia en el sistema permanece constante. Del mismo modo, cuando se evapora el agua, se convierte en vapor, pero la cantidad total de materia en el sistema sigue siendo la misma.
Comparación con tablas
Para comparar la ley de la conservación de la materia con las tablas, podemos pensar en las celdas de la tabla como átomos o moléculas individuales. Al igual que la ley de la conservación de la materia establece que la cantidad total de materia en un sistema cerrado permanece constante, las tablas tienen una cantidad fija de celdas que no pueden crearse ni destruirse. Sin embargo, al igual que la materia puede transformarse, las celdas de la tabla pueden cambiar de tamaño o contenido a medida que se actualiza el contenido.
listas
Las listas también se pueden comparar con la ley de la conservación de la materia. Al igual que la ley establece que la cantidad total de materia en un sistema cerrado permanece constante, las listas tienen un número fijo de elementos que no pueden crearse ni destruirse. Sin embargo, al igual que la materia puede transformarse, los elementos de la lista pueden cambiar de orden o contenido a medida que se actualiza el contenido.
Conclusión
La ley de la conservación de la materia es una regla fundamental de la química que establece que la cantidad total de materia en un sistema cerrado permanece constante a lo largo del tiempo. Esta ley se aplica en una amplia gama de situaciones, desde la combustión y la fotosíntesis hasta las reacciones químicas y los cambios de fase. Al entender y aplicar esta ley, podemos comprender mejor cómo funcionan los procesos químicos y cómo la materia se transforma en nuestro mundo.
Preguntas frecuentes
1. ¿Por qué es importante la ley de la conservación de la materia?
La ley de la conservación de la materia es importante porque nos ayuda a comprender cómo la materia se transforma y se mueve en nuestro mundo. Al entender esta ley, podemos predecir cómo se comportará la materia en diferentes situaciones y aplicar este conocimiento en áreas como la química, la física y la biología.
2. ¿Cómo se relaciona la ley de la conservación de la materia con la energía?
La ley de la conservación de la materia y la ley de la conservación de la energía están estrechamente relacionadas. Ambas leyes establecen que la cantidad total de materia o energía en un sistema cerrado permanece constante a lo largo del tiempo. Esto significa que la materia y la energía no pueden crearse ni destruirse, solo transformarse.
3. ¿Qué es un sistema cerrado?
Un sistema cerrado es un sistema en el que no hay intercambio de materia o energía con el entorno exterior. En un sistema cerrado, la cantidad total de materia o energía permanece constante a lo largo del tiempo.
4. ¿Cómo se aplica la ley de la conservación de la materia en la vida cotidiana?
La ley de la conservación de la materia se aplica en la vida cotidiana de muchas formas. Por ejemplo, cuando cocinamos, la cantidad total de materia en los ingredientes se conserva durante la cocción. Del mismo modo, cuando conducimos un automóvil, la cantidad total de materia en el combustible se conserva durante la combustión en el motor.
5. ¿Cuál es la relación entre la ley de la conservación de la materia y la ley de la conservación de la masa?
La ley de la conservación de la materia y la ley de la conservación de la masa son dos formas diferentes de expresar la misma regla fundamental de la química. La ley de la conservación de la materia se refiere a la conservación de la cantidad total de materia en un sistema cerrado, mientras que la ley de la conservación de la masa se refiere a la conservación de la masa total en un sistema cerrado. Ambas leyes establecen que la cantidad total de materia o masa no puede crearse ni destruirse, solo transformarse.

Deja una respuesta