Particula mas pequena de un elemento que presenta propiedades especificas
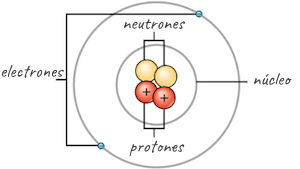
Si te preguntas cuál es la partícula más pequeña de un elemento que presenta propiedades específicas, la respuesta es el átomo. Los átomos son la unidad básica de la materia y están compuestos por protones, neutrones y electrones.
Cada elemento en la tabla periódica tiene un número atómico único, que representa la cantidad de protones en el núcleo de un átomo de ese elemento en particular. La cantidad de neutrones en el núcleo puede variar, lo que da lugar a diferentes isótopos del mismo elemento.
Los electrones orbitan alrededor del núcleo en capas o niveles de energía. Cada capa tiene un número máximo de electrones que puede contener y los electrones en la capa más externa son los que determinan las propiedades químicas de un elemento.
Por ejemplo, el hidrógeno tiene un solo electrón en su capa externa, lo que lo hace altamente reactivo y capaz de formar enlaces químicos con otros átomos para completar su capa de electrones. El oxígeno, por otro lado, tiene seis electrones en su capa externa y tiende a aceptar electrones de otros átomos para completar su capa.
La estructura atómica y la distribución de electrones son importantes para entender las propiedades físicas y químicas de los elementos. Por ejemplo, los elementos en la misma columna de la tabla periódica (conocidos como grupos) tienen propiedades químicas similares debido a que tienen la misma cantidad de electrones en su capa externa.
En resumen, El átomo es la partícula más pequeña de un elemento que presenta propiedades específicas. Su estructura atómica y la distribución de electrones son cruciales para entender las propiedades físicas y químicas de los elementos.
¿Cómo se descubrieron los átomos?
La idea de que la materia estaba compuesta por partículas indivisibles se remonta a la antigua Grecia, pero fue el químico británico John Dalton quien en el siglo XIX formuló la teoría moderna del átomo. Dalton propuso que los átomos eran esferas sólidas e indivisibles que se combinaban en proporciones simples para formar compuestos químicos.
Sin embargo, a medida que avanzaba la investigación científica, se descubrió que los átomos no eran indivisibles y que estaban compuestos por partículas subatómicas como protones, neutrones y electrones.
¿Cómo se mide el tamaño de los átomos?
El tamaño de un átomo se mide por su radio atómico, que es la distancia entre el centro del núcleo y el electrón más externo. Debido a que los electrones no están en una posición fija, el radio atómico puede variar según el átomo y el estado de oxidación.
En general, el radio atómico disminuye a medida que se mueve de izquierda a derecha en un período de la tabla periódica debido a un aumento en la carga nuclear efectiva (la atracción que siente el electrón hacia el núcleo), y aumenta a medida que se mueve hacia abajo en un grupo debido a la adición de niveles de energía.
¿Qué es un ion?
Un ion es un átomo o molécula que ha ganado o perdido uno o más electrones. Los iones con carga positiva se llaman cationes y los iones con carga negativa se llaman aniones.
La formación de iones es importante en la química porque los iones cargados pueden interactuar con otros iones y moléculas para formar compuestos químicos.
Tabla comparativa de átomos
| Elemento | Protones | Neutrones | Electrones | Radio atómico |
|---|---|---|---|---|
| Hidrógeno | 1 | 0 | 1 | 53 pm |
| Oxígeno | 8 | 8 | 8 | 73 pm |
| Carbono | 6 | 6 | 6 | 67 pm |
¿Por qué son importantes los átomos y su estructura?
La estructura atómica y la distribución de electrones son importantes para entender las propiedades físicas y químicas de los elementos, lo que a su vez es fundamental para la química, la física y la biología.
Por ejemplo, la comprensión de los átomos y las moléculas es esencial en la síntesis y fabricación de medicamentos y materiales avanzados. La estructura atómica también es fundamental para entender la energía nuclear, la electricidad y la electrónica.
¿Cómo se representan los átomos?
Los átomos se representan mediante símbolos químicos, que indican el elemento químico y su número atómico. Por ejemplo, el símbolo químico para el hidrógeno es H y su número atómico es 1, lo que significa que tiene un solo protón en su núcleo.
Además de los símbolos químicos, los átomos se representan mediante modelos atómicos, que pueden ser modelos de bolas y varillas, modelos de nubes electrónicas o modelos de orbitales atómicos.
Conclusión
Los átomos son la unidad básica de la materia y están compuestos por protones, neutrones y electrones. La estructura atómica y la distribución de electrones son importantes para entender las propiedades físicas y químicas de los elementos. La comprensión de los átomos y las moléculas es esencial en la síntesis y fabricación de medicamentos y materiales avanzados, así como en la energía nuclear, la electricidad y la electrónica. Los átomos se representan mediante símbolos químicos y modelos atómicos.

Deja una respuesta