Porque la electronegatividad aumenta a lo largo de un periodo
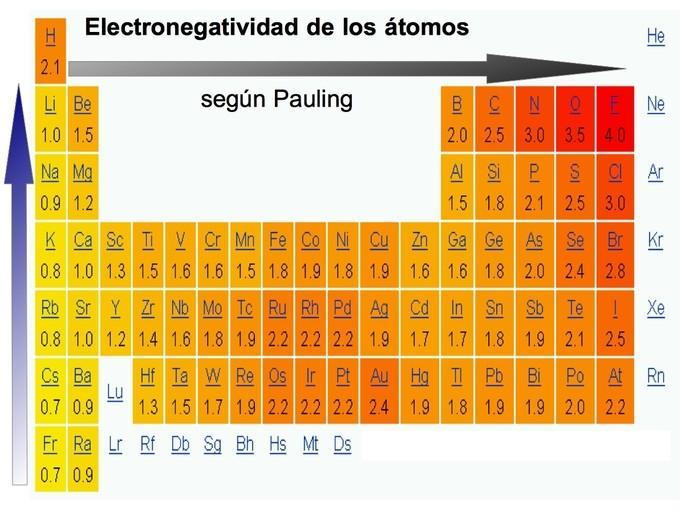
La electronegatividad es una propiedad química que mide la capacidad de un átomo de atraer electrones hacia sí mismo cuando forma un enlace químico con otro átomo. Esta propiedad varía en función de la posición del elemento en la tabla periódica. En este artículo, explicaremos por qué la electronegatividad aumenta a lo largo de un periodo.
- ¿Qué es un periodo en la tabla periódica?
- ¿Qué es la electronegatividad?
- ¿Por qué la electronegatividad aumenta a lo largo de un periodo?
- ¿Qué otros factores influyen en la electronegatividad?
- Conclusión
- Preguntas frecuentes
- 1. ¿Qué es la carga nuclear efectiva?
- 2. ¿Qué otros factores influyen en la electronegatividad?
- 3. ¿Por qué los elementos en un grupo tienen la misma electronegatividad?
- 4. ¿Qué es un periodo en la tabla periódica?
- 5. ¿Cómo se compara el aumento de la electronegatividad a lo largo de un periodo con una tabla HTML?
¿Qué es un periodo en la tabla periódica?
Antes de explicar por qué la electronegatividad aumenta a lo largo de un periodo, es importante entender qué es un periodo en la tabla periódica. Los periodos son las filas horizontales en la tabla periódica, y representan el número de niveles de energía que tienen los electrones en los átomos de los elementos en esa fila.
¿Qué es la electronegatividad?
La electronegatividad es una propiedad química que mide la capacidad de un átomo de atraer electrones hacia sí mismo cuando forma un enlace químico con otro átomo. Los átomos con alta electronegatividad tienen una gran capacidad de atraer electrones, mientras que los átomos con baja electronegatividad tienen una menor capacidad de hacerlo.
¿Por qué la electronegatividad aumenta a lo largo de un periodo?
La electronegatividad aumenta a lo largo de un periodo debido a la carga nuclear efectiva. La carga nuclear efectiva es la fuerza con la que el núcleo atrae a los electrones en un átomo. A medida que avanzamos de izquierda a derecha en un periodo, el número de protones en el núcleo aumenta, lo que significa que la carga nuclear efectiva también aumenta. Esto hace que los electrones en los átomos de los elementos en un periodo sean atraídos con mayor fuerza hacia el núcleo, lo que aumenta la electronegatividad.
Comparación con tablas
Podemos comparar el aumento de la electronegatividad a lo largo de un periodo con una tabla HTML. Al igual que una tabla HTML tiene celdas que se ordenan de izquierda a derecha, los elementos en un periodo se ordenan de izquierda a derecha. Al avanzar de una celda a la siguiente en una tabla HTML, se puede observar cómo cambian los valores. De manera similar, al avanzar de un elemento a otro en un periodo, se puede observar cómo cambia la electronegatividad.
¿Qué otros factores influyen en la electronegatividad?
Además de la carga nuclear efectiva, hay otros factores que influyen en la electronegatividad. Uno de ellos es el tamaño del átomo. A medida que el tamaño del átomo aumenta, la electronegatividad disminuye debido a que los electrones están más lejos del núcleo y son menos atraídos hacia él. Otro factor que influye en la electronegatividad es la polaridad del enlace químico. Los átomos con una gran diferencia en electronegatividad forman enlaces más polarizados, lo que significa que los electrones se comparten de manera desigual y se atraen con mayor fuerza hacia el átomo más electronegativo.
Conclusión
La electronegatividad es una propiedad química importante que mide la capacidad de un átomo de atraer electrones hacia sí mismo cuando forma un enlace químico con otro átomo. A medida que avanzamos de izquierda a derecha en un periodo en la tabla periódica, el número de protones en el núcleo aumenta, lo que significa que la carga nuclear efectiva también aumenta. Esto hace que los electrones en los átomos de los elementos en un periodo sean atraídos con mayor fuerza hacia el núcleo, lo que aumenta la electronegatividad.
Preguntas frecuentes
1. ¿Qué es la carga nuclear efectiva?
La carga nuclear efectiva es la fuerza con la que el núcleo atrae a los electrones en un átomo. A medida que aumenta el número de protones en el núcleo, la carga nuclear efectiva aumenta, lo que significa que los electrones son atraídos con mayor fuerza hacia el núcleo.
2. ¿Qué otros factores influyen en la electronegatividad?
Además de la carga nuclear efectiva, el tamaño del átomo y la polaridad del enlace químico también influyen en la electronegatividad.
3. ¿Por qué los elementos en un grupo tienen la misma electronegatividad?
Los elementos en un grupo tienen la misma electronegatividad debido a que tienen el mismo número de electrones en su capa exterior, lo que significa que tienen una estructura electrónica similar.
4. ¿Qué es un periodo en la tabla periódica?
Un periodo es una fila horizontal en la tabla periódica que representa el número de niveles de energía que tienen los electrones en los átomos de los elementos en esa fila.
5. ¿Cómo se compara el aumento de la electronegatividad a lo largo de un periodo con una tabla HTML?
Al igual que una tabla HTML tiene celdas que se ordenan de izquierda a derecha, los elementos en un periodo se ordenan de izquierda a derecha. Al avanzar de una celda a la siguiente en una tabla HTML, se puede observar cómo cambian los valores. De manera similar, al avanzar de un elemento a otro en un periodo, se puede observar cómo cambia la electronegatividad.

Deja una respuesta