Que expresa la ley de la conservacion de la materia
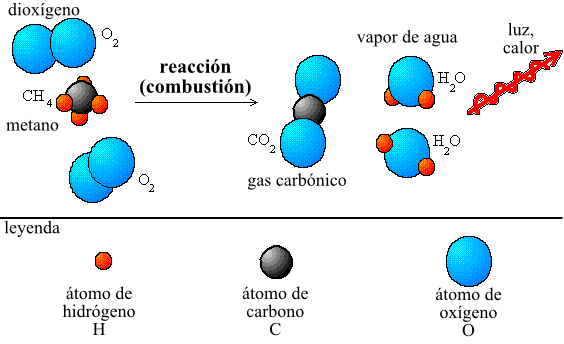
La ley de la conservación de la materia, también conocida como ley de la conservación de la masa, es uno de los pilares fundamentales de la química. Esta ley establece que en un sistema cerrado, la masa total de los componentes es constante, es decir, la masa no se crea ni se destruye, simplemente se transforma.
Esta ley fue propuesta por el químico francés Antoine Lavoisier en el siglo XVIII, quien realizó una serie de experimentos en los que demostró que la masa de los reactivos era igual a la masa de los productos obtenidos después de una reacción química. Esto llevó a la conclusión de que la materia no podía ser creada ni destruida, sino que simplemente cambiaba de forma.
En términos más simples, esto significa que si tomamos un bloque de hielo y lo dejamos a temperatura ambiente, se derretirá convirtiéndose en agua. Aunque el bloque de hielo ha cambiado de forma, la cantidad de materia que lo compone sigue siendo la misma. De igual manera, si quemamos una hoja de papel, la materia de la hoja se transforma en ceniza, pero la masa total sigue siendo la misma.
La ley de la conservación de la materia es aplicable a cualquier tipo de sistema, ya sea una reacción química, una combustión, una descomposición o cualquier otro proceso que implique la transformación de la materia. Esta ley es fundamental en la química, ya que nos permite predecir el resultado de una reacción química y calcular la cantidad de producto que se obtendrá.
La ley de la conservación de la materia también tiene implicaciones importantes en la vida cotidiana. Por ejemplo, cuando se produce una explosión, la materia se transforma en gases y partículas, pero la masa total sigue siendo la misma. De igual manera, cuando se cocina un alimento, la materia se transforma en otra forma (como cuando se cuece un huevo), pero la masa total sigue siendo la misma.
En resumen, La ley de la conservación de la materia expresa que la masa total de los componentes de un sistema cerrado es constante, lo que significa que la materia no se crea ni se destruye, simplemente se transforma. Esta ley es fundamental en la química y tiene implicaciones importantes en la vida cotidiana.
- ¿Cómo se aplica la ley de la conservación de la materia en la química?
- ¿Por qué es importante la ley de la conservación de la materia en la vida cotidiana?
- ¿Cómo se relaciona la ley de la conservación de la materia con otras leyes de la física y la química?
- ¿Qué pasaría si la ley de la conservación de la materia no fuera cierta?
- ¿Cómo se puede demostrar la ley de la conservación de la materia en un experimento?
¿Cómo se aplica la ley de la conservación de la materia en la química?
La ley de la conservación de la materia se aplica en la química en cualquier tipo de sistema que implique la transformación de la materia. Por ejemplo, en una reacción química, los reactivos se combinan para formar productos. En este proceso, la cantidad de materia que se transforma es constante, lo que significa que la masa total de los reactivos es igual a la masa total de los productos.
Para aplicar la ley de la conservación de la materia en una reacción química, es necesario equilibrar la ecuación química para asegurarse de que la cantidad de átomos de cada elemento es la misma en ambos lados de la ecuación. De esta manera, se puede calcular la cantidad de reactivo que se necesita para obtener una cantidad específica de producto.
¿Por qué es importante la ley de la conservación de la materia en la vida cotidiana?
La ley de la conservación de la materia es importante en la vida cotidiana porque nos permite comprender cómo funciona el mundo que nos rodea. Esta ley nos muestra que aunque los objetos puedan cambiar de forma, la cantidad de materia que los compone sigue siendo la misma.
Por ejemplo, cuando cocinamos un alimento, la materia se transforma en otra forma, como cuando se cuece un huevo. Sin embargo, la masa total del huevo sigue siendo la misma antes y después de la cocción. De igual manera, cuando se produce una explosión, la materia se transforma en gases y partículas, pero la masa total sigue siendo la misma.
¿Cómo se relaciona la ley de la conservación de la materia con otras leyes de la física y la química?
La ley de la conservación de la materia se relaciona con otras leyes de la física y la química, como la ley de la conservación de la energía y la ley de las proporciones definidas.
La ley de la conservación de la energía establece que la energía no se crea ni se destruye, sino que se transforma, al igual que la materia. Por lo tanto, los procesos químicos y físicos que involucran la transformación de la materia también involucran la transformación de la energía.
La ley de las proporciones definidas establece que los elementos que forman un compuesto siempre están presentes en una proporción fija y definida. Esta ley se relaciona con la ley de la conservación de la materia porque, en una reacción química, la cantidad total de materia que se transforma es constante.
¿Qué pasaría si la ley de la conservación de la materia no fuera cierta?
Si la ley de la conservación de la materia no fuera cierta, significaría que la cantidad de materia en el universo podría cambiar de forma aleatoria. Esto tendría consecuencias dramáticas, ya que cualquier cosa que se creara o se destruyera tendría un impacto directo en la cantidad total de materia que existe en el universo.
Por ejemplo, si la materia pudiera ser creada a partir de la nada, esto significaría que la cantidad total de materia en el universo podría aumentar de forma ilimitada. Esto tendría implicaciones importantes en la física y la cosmología, ya que la cantidad de materia en el universo es un factor clave en la comprensión de la estructura y evolución del cosmos.
¿Cómo se puede demostrar la ley de la conservación de la materia en un experimento?
La ley de la conservación de la materia se puede demostrar en un experimento sencillo utilizando una balanza y algunos productos químicos. Por ejemplo, si se mezcla bicarbonato de sodio con ácido clorhídrico, se produce una reacción química que genera dióxido de carbono y cloruro de sodio.
Para demostrar la ley de la conservación de la materia en este experimento, se puede medir la masa total de los reactivos (bicarbonato de sodio y ácido clorhídrico) antes de la reacción y la masa total de los productos (dióxido de carbono y cloruro de sodio) después de la reacción. Si la ley de la conservación de la materia es cierta, la masa total de los reactivos debe ser igual a la masa total de los productos.

Deja una respuesta