Que pasa si aumenta la temperatura en una reaccion quimica
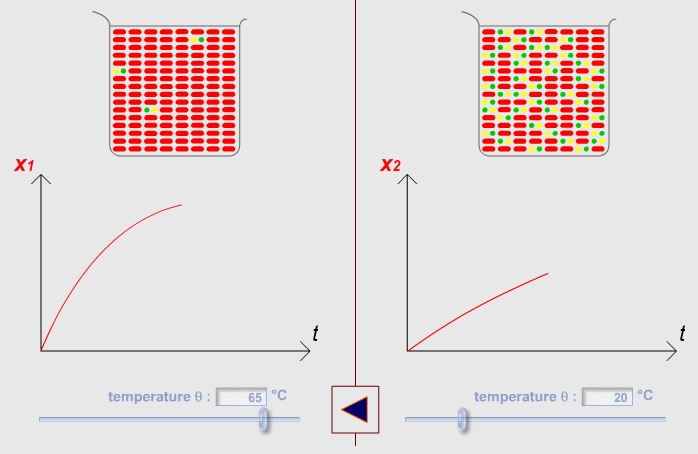
Las reacciones químicas son procesos complejos que ocurren cuando dos o más sustancias interactúan para formar nuevos compuestos. Uno de los factores que más influyen en estas reacciones es la temperatura. En este artículo, exploraremos qué sucede cuando se aumenta la temperatura en una reacción química.
- ¿Cómo afecta la temperatura a las reacciones químicas?
- ¿Qué sucede cuando aumenta la temperatura en una reacción exotérmica?
- ¿Qué sucede cuando aumenta la temperatura en una reacción endotérmica?
- ¿Cómo afecta la temperatura al equilibrio químico?
- ¿Cómo se puede controlar la temperatura en una reacción química?
- Conclusión
- Preguntas frecuentes
¿Cómo afecta la temperatura a las reacciones químicas?
La temperatura es un factor crítico en las reacciones químicas. A medida que se aumenta la temperatura, se incrementa la energía cinética de las moléculas. Esto significa que las moléculas se mueven más rápidamente y colisionan con más frecuencia y con mayor energía.
Cuando las moléculas colisionan, pueden intercambiar electrones y enlaces químicos, lo que puede producir una reacción química. Si la temperatura es lo suficientemente alta, esta energía adicional puede romper enlaces químicos, lo que puede llevar a la formación de nuevos compuestos.
¿Qué sucede cuando aumenta la temperatura en una reacción exotérmica?
Una reacción exotérmica es aquella que libera energía en forma de calor. Cuando se aumenta la temperatura en una reacción exotérmica, se acelera la liberación de calor. Esto puede aumentar la velocidad de la reacción y hacer que se complete más rápidamente.
Por otro lado, si la temperatura es demasiado alta, puede ocurrir lo contrario. Si la reacción ya ha liberado la cantidad máxima de calor posible, aumentar la temperatura puede disminuir la velocidad de la reacción porque la energía adicional no puede ser absorbida por la reacción.
¿Qué sucede cuando aumenta la temperatura en una reacción endotérmica?
Una reacción endotérmica es aquella que absorbe energía en forma de calor. Cuando se aumenta la temperatura en una reacción endotérmica, se aumenta la cantidad de energía disponible para la reacción. Esto puede aumentar la velocidad de la reacción y hacer que se complete más rápidamente.
Sin embargo, si la temperatura es demasiado alta, puede ocurrir lo contrario. Si la reacción ya ha absorbido la cantidad máxima de calor posible, aumentar la temperatura puede disminuir la velocidad de la reacción porque la energía adicional no puede ser absorbida por la reacción.
¿Cómo afecta la temperatura al equilibrio químico?
En una reacción química en equilibrio, la velocidad de la reacción en la dirección hacia los productos es igual a la velocidad de la reacción en la dirección hacia los reactivos. Si se aumenta la temperatura en una reacción en equilibrio, la velocidad de ambas reacciones aumentará.
Esto puede desplazar el equilibrio hacia la dirección de la reacción endotérmica, lo que significa que se formarán más productos. Si la temperatura es lo suficientemente alta, la reacción endotérmica puede ser la reacción predominante.
Por otro lado, si se disminuye la temperatura en una reacción en equilibrio, la velocidad de ambas reacciones disminuirá. Esto puede desplazar el equilibrio hacia la dirección de la reacción exotérmica, lo que significa que se formarán más reactivos.
¿Cómo se puede controlar la temperatura en una reacción química?
La temperatura en una reacción química puede ser controlada de diversas maneras. Una forma común es mediante la adición de un reactivo a la solución que absorba o libere calor. Estos reactivos se conocen como reactivos termoquímicos.
Otra forma es mediante el uso de un baño de agua o aceite caliente o frío para mantener la temperatura constante. También se pueden utilizar equipos más avanzados, como hornos de alta temperatura o cámaras de reacción controladas por ordenador.
Conclusión
La temperatura es un factor crítico en las reacciones químicas. A medida que se aumenta la temperatura, se incrementa la energía cinética de las moléculas, lo que puede llevar a la formación de nuevos compuestos. Sin embargo, si la temperatura es demasiado alta, puede disminuir la velocidad de la reacción. Es importante controlar la temperatura en las reacciones químicas para garantizar una reacción eficiente y segura.
Preguntas frecuentes
¿Cómo afecta la temperatura a la velocidad de una reacción química?
La temperatura afecta la velocidad de una reacción química al aumentar la energía cinética de las moléculas, lo que puede llevar a la formación de nuevos compuestos. Si la temperatura es demasiado alta, puede disminuir la velocidad de la reacción.
¿Qué es una reacción exotérmica?
Una reacción exotérmica es aquella que libera energía en forma de calor.
¿Qué es una reacción endotérmica?
Una reacción endotérmica es aquella que absorbe energía en forma de calor.
¿Cómo se puede controlar la temperatura en una reacción química?
La temperatura en una reacción química puede ser controlada de diversas maneras, como mediante la adición de un reactivo termoquímico o mediante el uso de un baño de agua o aceite caliente o frío.
¿Cómo afecta la temperatura al equilibrio químico?
Si se aumenta la temperatura en una reacción en equilibrio, la velocidad de ambas reacciones aumentará. Esto puede desplazar el equilibrio hacia la dirección de la reacción endotérmica, lo que significa que se formarán más productos. Si se disminuye la temperatura en una reacción en equilibrio, la velocidad de ambas reacciones disminuirá y puede desplazar el equilibrio hacia la dirección de la reacción exotérmica.

Deja una respuesta