Que procesos termodinamicos se presentan en la primera ley de la termodinamica
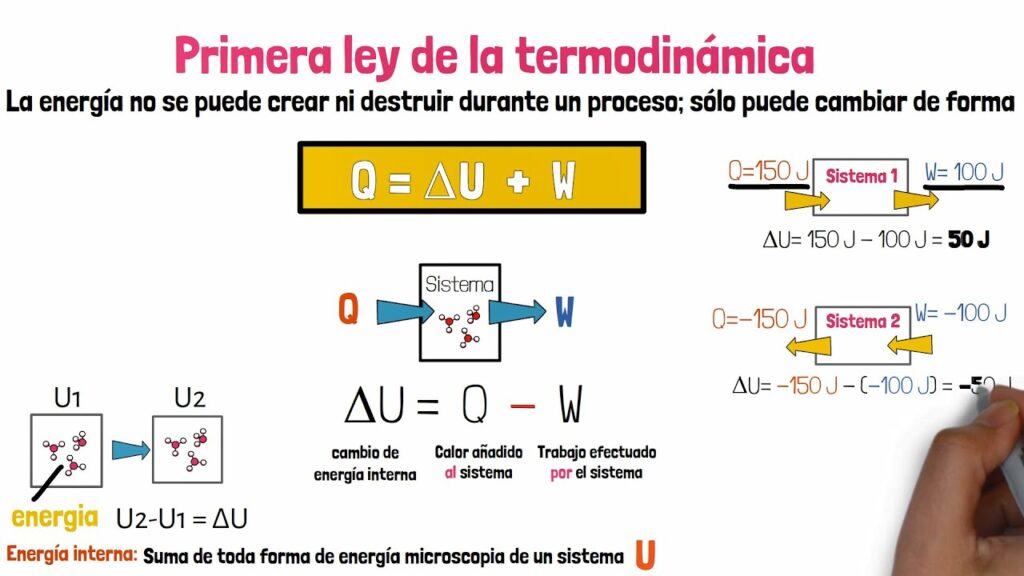
La termodinámica es una rama de la física que se encarga de estudiar los procesos relacionados con la transferencia de calor y energía. La primera ley de la termodinámica, también conocida como el principio de conservación de la energía, establece que la energía no se crea ni se destruye, solo se transforma. En este artículo, hablaremos sobre los procesos termodinámicos que se presentan en la primera ley de la termodinámica.
Procesos termodinámicos
Los procesos termodinámicos son aquellos que ocurren en un sistema termodinámico y que implican cambios en la energía interna, la temperatura o la presión. Estos procesos pueden ser clasificados en cuatro tipos: adiabáticos, isotérmicos, isobáricos e isocóricos.
Procesos adiabáticos
Un proceso adiabático es aquel que no involucra transferencia de calor entre el sistema y su entorno. En otras palabras, la energía no fluye hacia el sistema desde el exterior ni sale del sistema hacia el exterior durante el proceso. Un ejemplo de proceso adiabático es la compresión o expansión rápida de un gas en un cilindro con un pistón.
Procesos isotérmicos
Un proceso isotérmico es aquel en el que la temperatura del sistema permanece constante. En un proceso isotérmico, la energía térmica que se agrega al sistema se convierte en trabajo mecánico realizado por el sistema. Un ejemplo de proceso isotérmico es la expansión de un gas en un motor de combustión interna.
Procesos isobáricos
Un proceso isobárico es aquel en el que la presión del sistema permanece constante. En un proceso isobárico, la energía térmica que se agrega al sistema se convierte en trabajo mecánico realizado por el sistema. Un ejemplo de proceso isobárico es la cocción de alimentos en una olla a presión.
Procesos isocóricos
Un proceso isocórico es aquel en el que el volumen del sistema permanece constante. En un proceso isocórico, la energía térmica que se agrega al sistema se convierte en un aumento de la temperatura del sistema. Un ejemplo de proceso isocórico es la combustión de un combustible en un motor de combustión interna.
Comparación con tablas
Para entender mejor estos procesos termodinámicos, podemos compararlos con tablas. Al igual que HTML tiene diferentes etiquetas para diferentes tipos de contenido, los procesos termodinámicos también tienen diferentes tipos según los cambios en energía, temperatura y presión.
Etiqueta adiabática
La etiqueta adiabática en HTML sería aquella que no permite la transferencia de energía entre los elementos de la página. Del mismo modo, un proceso termodinámico adiabático no permite la transferencia de energía entre el sistema y su entorno.
Etiqueta isotérmica
La etiqueta isotérmica en HTML sería aquella que mantiene una temperatura constante en los elementos de la página, independientemente de los cambios en el entorno. De manera similar, un proceso termodinámico isotérmico mantiene una temperatura constante en el sistema, independientemente de los cambios en el entorno.
Etiqueta isobárica
La etiqueta isobárica en HTML sería aquella que mantiene una presión constante en los elementos de la página, independientemente de los cambios en el entorno. De manera similar, un proceso termodinámico isobárico mantiene una presión constante en el sistema, independientemente de los cambios en el entorno.
Etiqueta isocórica
La etiqueta isocórica en HTML sería aquella que mantiene un volumen constante en los elementos de la página, independientemente de los cambios en el entorno. De manera similar, un proceso termodinámico isocórico mantiene un volumen constante en el sistema, independientemente de los cambios en el entorno.
listas
Otra forma de entender estos procesos termodinámicos es a través de listas.
- Proceso adiabático:
- No hay transferencia de energía.
- No hay cambio en la temperatura.
- No hay cambio en la presión.
- No hay cambio en el volumen.
- Proceso isotérmico:
- No hay transferencia de energía.
- La temperatura permanece constante.
- No hay cambio en la presión.
- El volumen cambia.
- Proceso isobárico:
- No hay transferencia de energía.
- No hay cambio en la temperatura.
- La presión permanece constante.
- El volumen cambia.
- Proceso isocórico:
- No hay transferencia de energía.
- La temperatura cambia.
- No hay cambio en la presión.
- El volumen permanece constante.
Conclusión
En resumen, La primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma. Los procesos termodinámicos que se presentan en la primera ley son adiabáticos, isotérmicos, isobáricos e isocóricos. Cada uno de estos procesos tiene diferentes características y efectos sobre la energía, la temperatura, la presión y el volumen del sistema.
Preguntas frecuentes
¿Qué es la termodinámica?
La termodinámica es una rama de la física que se encarga de estudiar los procesos relacionados con la transferencia de calor y energía.
¿Qué establece la primera ley de la termodinámica?
La primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma.
¿Cuáles son los procesos termodinámicos que se presentan en la primera ley?
Los procesos termodinámicos que se presentan en la primera ley son adiabáticos, isotérmicos, isobáricos e isocóricos.
¿Qué es un proceso adiabático?
Un proceso adiabático es aquel que no involucra transferencia de calor entre el sistema y su entorno.
¿Qué es un proceso isotérmico?
Un proceso isotérmico es aquel en el que la temperatura del sistema permanece constante.

Deja una respuesta