Que tipo de enlace covalente es el dioxido de carbono
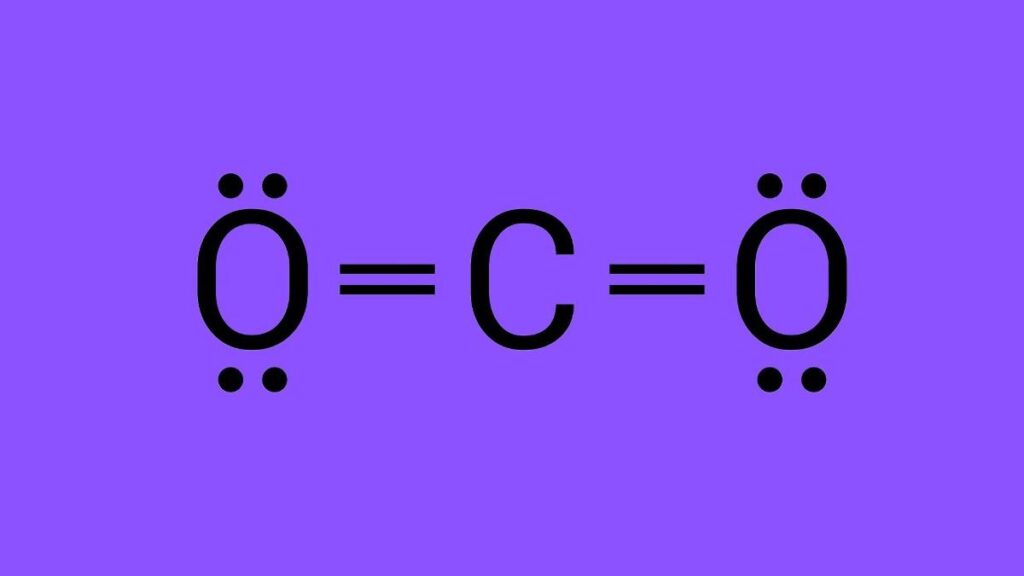
El dióxido de carbono, o CO2, es una molécula compuesta por dos átomos de oxígeno y un átomo de carbono. La pregunta que surge es qué tipo de enlace covalente existe en esta molécula. Para entender esto, primero hay que entender qué es un enlace covalente.
Un enlace covalente es un tipo de enlace químico en el que dos átomos comparten electrones para formar una molécula estable. Hay dos tipos de enlaces covalentes: enlace covalente polar y enlace covalente no polar.
En un enlace covalente polar, los electrones compartidos no son compartidos equitativamente entre los dos átomos. En cambio, un átomo atrae más electrones que el otro, lo que resulta en una distribución desigual de la carga eléctrica en la molécula.
En un enlace covalente no polar, los electrones compartidos son compartidos equitativamente entre los dos átomos, lo que resulta en una distribución uniforme de la carga eléctrica en la molécula.
Entonces, ¿qué tipo de enlace covalente es el dióxido de carbono? El CO2 es un ejemplo de un enlace covalente no polar. Esto se debe a que los átomos de oxígeno y carbono comparten electrones de manera equitativa, lo que resulta en una distribución uniforme de la carga eléctrica en la molécula.
Es importante tener en cuenta que, aunque el enlace covalente en el dióxido de carbono es no polar, la molécula en sí puede ser polar debido a la forma en que los átomos están dispuestos en la molécula. Esto se debe a que los átomos de oxígeno atraen más electrones que el átomo de carbono, lo que resulta en una distribución desigual de la carga eléctrica en la molécula.
En resumen, El dióxido de carbono es un ejemplo de un enlace covalente no polar debido a la forma en que los átomos de oxígeno y carbono comparten electrones. Sin embargo, la molécula en sí puede ser polar debido a la disposición de los átomos en la molécula.
Comparación con tablas
Para comprender mejor la diferencia entre un enlace covalente polar y no polar, se puede utilizar una tabla HTML como herramienta de comparación.
| Enlace covalente polar | Enlace covalente no polar |
|---|---|
| Los electrones compartidos no son compartidos equitativamente entre dos átomos | Los electrones compartidos son compartidos equitativamente entre dos átomos |
| Resulta en una distribución desigual de la carga eléctrica en la molécula | Resulta en una distribución uniforme de la carga eléctrica en la molécula |
| Ejemplo: agua (H2O) | Ejemplo: dióxido de carbono (CO2) |
Usando analogías para entender los enlaces covalentes
Para aquellos que tienen dificultades para comprender los enlaces covalentes, se pueden utilizar analogías para ayudar a entender los conceptos básicos.
Imagina que dos amigos están compartiendo una pizza. Si ambos amigos tienen el mismo apetito, compartirán la pizza de manera equitativa y cada uno recibirá la misma cantidad de pizza. Esto es similar a cómo funcionan los enlaces covalentes no polares, donde ambos átomos comparten electrones de manera equitativa.
Por otro lado, si uno de los amigos tiene más hambre que el otro, puede tomar más pizza para sí mismo y dejar menos para el otro amigo. Esto es similar a cómo funcionan los enlaces covalentes polares, donde un átomo atrae más electrones que el otro, lo que resulta en una distribución desigual de la carga eléctrica en la molécula.
Lista HTML: claves para entender los enlaces covalentes
- Los enlaces covalentes son un tipo de enlace químico en el que dos átomos comparten electrones para formar una molécula estable
- Hay dos tipos de enlaces covalentes: enlace covalente polar y enlace covalente no polar
- En un enlace covalente polar, los electrones compartidos no son compartidos equitativamente entre los dos átomos
- En un enlace covalente no polar, los electrones compartidos son compartidos equitativamente entre los dos átomos
- El dióxido de carbono es un ejemplo de un enlace covalente no polar debido a la forma en que los átomos de oxígeno y carbono comparten electrones
- Aunque el enlace covalente en el dióxido de carbono es no polar, la molécula en sí puede ser polar debido a la forma en que los átomos están dispuestos en la molécula
Preguntas frecuentes
¿Qué es un enlace covalente?
Un enlace covalente es un tipo de enlace químico en el que dos átomos comparten electrones para formar una molécula estable.
¿Cuáles son los dos tipos de enlaces covalentes?
Los dos tipos de enlaces covalentes son enlace covalente polar y enlace covalente no polar.
¿Qué es un enlace covalente no polar?
En un enlace covalente no polar, los electrones compartidos son compartidos equitativamente entre los dos átomos, lo que resulta en una distribución uniforme de la carga eléctrica en la molécula.
¿Qué es un enlace covalente polar?
En un enlace covalente polar, los electrones compartidos no son compartidos equitativamente entre los dos átomos. En cambio, un átomo atrae más electrones que el otro, lo que resulta en una distribución desigual de la carga eléctrica en la molécula.
¿Es el dióxido de carbono un ejemplo de un enlace covalente polar o no polar?
El dióxido de carbono es un ejemplo de un enlace covalente no polar debido a la forma en que los átomos de oxígeno y carbono comparten electrones. Sin embargo, la molécula en sí puede ser polar debido a la disposición de los átomos en la molécula.

Deja una respuesta