Termodinamica temperatura calor y primera ley de la termodinamica
La termodinámica es una rama de la física que se encarga del estudio de la relación entre la energía y la temperatura en un sistema. Esta disciplina es de gran importancia en el mundo actual, ya que nos permite entender cómo funcionan los procesos energéticos en nuestra vida diaria, como por ejemplo en la generación de energía eléctrica o en el diseño de motores de combustión interna.
En este artículo, hablaremos sobre tres conceptos fundamentales de la termodinámica: la temperatura, el calor y la primera ley de la termodinámica.
¿Qué es la temperatura?
La temperatura es una medida de la energía cinética promedio de las moléculas en un sistema. En otras palabras, es una medida de la intensidad del calor en un cuerpo. La unidad de medida de la temperatura es el grado Celsius (°C), aunque también se puede utilizar el kelvin (K) en la termodinámica.
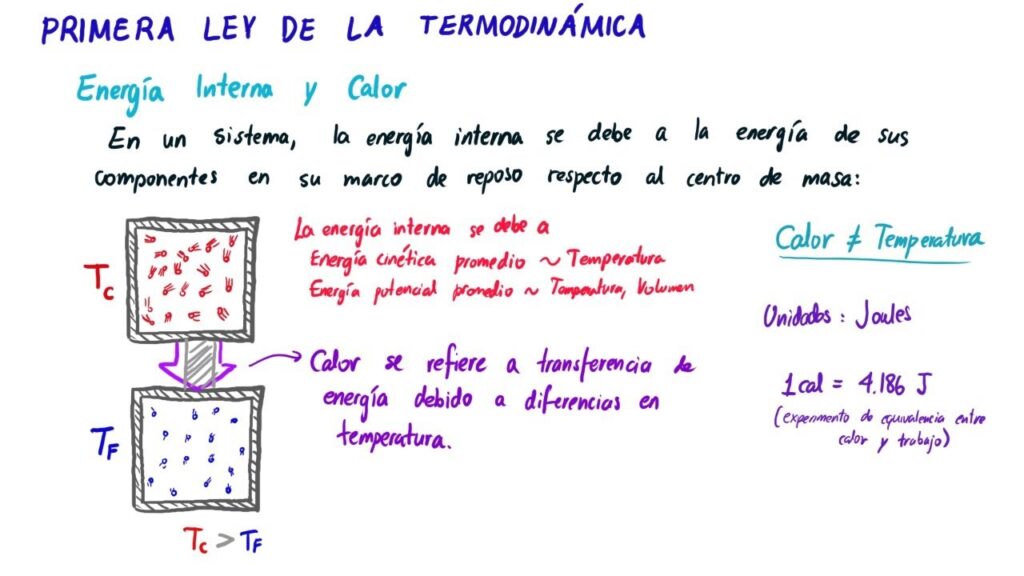
Es importante tener en cuenta que la temperatura no es lo mismo que el calor. Mientras que la temperatura es una medida de la energía cinética de las moléculas, el calor es una forma de energía que se transfiere de un cuerpo a otro debido a una diferencia de temperatura.
¿Qué es el calor?
El calor es una forma de energía que fluye de un cuerpo a otro debido a una diferencia de temperatura. Cuando dos cuerpos que están a diferentes temperaturas entran en contacto, el calor fluirá del cuerpo más caliente al cuerpo más frío hasta que ambos cuerpos alcancen la misma temperatura.
La cantidad de calor que se transfiere de un cuerpo a otro depende de la diferencia de temperatura entre ambos cuerpos y de las propiedades del material de los cuerpos.
¿Qué es la primera ley de la termodinámica?
La primera ley de la termodinámica es una ley fundamental que establece que la energía no se crea ni se destruye, sino que se transforma de una forma a otra. En otras palabras, la cantidad total de energía en un sistema cerrado permanece constante.
En el contexto de la termodinámica, la primera ley establece que la cantidad de calor que se transfiere a un sistema más la cantidad de trabajo que se realiza en el sistema es igual a la variación de la energía interna del sistema. Esta ley es fundamental para entender cómo funcionan los procesos energéticos en la naturaleza y en la tecnología.
¿Cómo se relacionan la temperatura, el calor y la primera ley de la termodinámica?
La relación entre la temperatura, el calor y la primera ley de la termodinámica es fundamental para entender cómo los procesos energéticos funcionan en el mundo. Cuando se transfiere calor a un sistema, la temperatura del sistema aumenta y su energía interna también aumenta. Si se realiza trabajo en el sistema (por ejemplo, al comprimir un gas), la energía interna del sistema también puede aumentar.
La primera ley de la termodinámica establece que la variación de la energía interna de un sistema es igual a la cantidad de calor que se transfiere a él más la cantidad de trabajo que se realiza en él. Esto significa que si se transfiere calor a un sistema y se realiza trabajo en él, la energía interna del sistema aumentará.
Conclusión
La termodinámica es una disciplina fundamental para entender cómo funciona la energía en nuestro mundo. La temperatura, el calor y la primera ley de la termodinámica son conceptos clave que nos permiten entender cómo la energía fluye y se transforma en los sistemas.
Preguntas frecuentes
1. ¿Cómo se mide la temperatura?
La temperatura se mide en grados Celsius (°C) o en kelvin (K) utilizando termómetros o sensores de temperatura.
2. ¿Qué es la entalpía?
La entalpía es una propiedad termodinámica que describe la cantidad total de energía de un sistema a una presión constante.
3. ¿Qué es un proceso isobárico?
Un proceso isobárico es un proceso termodinámico en el que la presión del sistema se mantiene constante mientras se realiza trabajo en el sistema.
4. ¿Qué es un proceso adiabático?
Un proceso adiabático es un proceso termodinámico en el que no se transfiere calor entre el sistema y el entorno.
5. ¿Qué es la segunda ley de la termodinámica?
La segunda ley de la termodinámica establece que la entropía de un sistema cerrado nunca disminuye con el tiempo. En otras palabras, todos los procesos naturales tienden a aumentar la desorden y la irreversibilidad.

Deja una respuesta