Porque un cubo de hielo cambia de solido a liquido
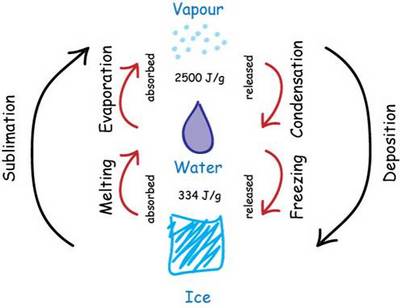
Cuando ponemos un cubo de hielo en una bebida, esperamos que se derrita y se convierta en líquido. Pero, ¿por qué ocurre este cambio de estado tan común en nuestro día a día?
Para entenderlo, primero necesitamos conocer las propiedades de la materia y cómo se relacionan con la energía. Todos los objetos están compuestos por partículas en constante movimiento: los átomos y las moléculas. En los sólidos, estas partículas están muy cerca unas de otras y se mantienen en una estructura fija, por lo que el objeto mantiene su forma y volumen. En los líquidos, las partículas están más separadas y se mueven libremente, por lo que el objeto adopta la forma del recipiente en el que se encuentra, pero mantiene su volumen. En los gases, las partículas están muy separadas y se mueven rápidamente, por lo que el objeto adopta la forma y el volumen del recipiente que lo contiene.
El cambio de estado de un objeto se produce cuando se añade o se quita energía, lo que afecta la velocidad y la distancia entre las partículas. En el caso del hielo, es un sólido a temperatura ambiente porque las moléculas de agua están unidas en una estructura cristalina. Pero al añadir calor, ya sea a través de la temperatura ambiente o al ponerlo en una bebida caliente, las moléculas empiezan a vibrar más y a separarse un poco. Cuando la temperatura alcanza el punto de fusión, que es de 0 grados Celsius para el agua, las moléculas tienen suficiente energía para romper las uniones que las mantenían fijas en la estructura cristalina y empezar a moverse libremente. Por lo tanto, el hielo se convierte en agua líquida.
Este proceso se llama fusión y es un ejemplo de un cambio de estado de sólido a líquido. El proceso inverso, de líquido a sólido, se llama solidificación y ocurre cuando se quita energía del líquido, por ejemplo, al poner agua en un congelador. Cuando la temperatura baja del punto de congelación, que también es de 0 grados Celsius para el agua, las moléculas empiezan a agruparse y a formar una estructura cristalina, lo que resulta en hielo sólido.
En resumen, Un cubo de hielo cambia de sólido a líquido cuando se añade suficiente energía para que las moléculas de agua empiecen a moverse libremente y rompan las uniones que las mantenían fijas en la estructura cristalina. Este proceso se llama fusión y es un ejemplo de un cambio de estado de sólido a líquido debido a la energía añadida.
¿Cómo se puede calcular la cantidad de energía necesaria para derretir un cubo de hielo?
La cantidad de energía necesaria para derretir un cubo de hielo depende de la masa del hielo y de la cantidad de calor que se le añada. La ecuación que se utiliza para calcular la cantidad de energía necesaria es Q = m x c x deltaT, donde Q es la cantidad de energía en julios, m es la masa en kilogramos, c es la capacidad calorífica específica del agua (4,18 J/gC) y deltaT es el cambio de temperatura en grados Celsius. Para derretir completamente un cubo de hielo de 100 gramos, que tiene una temperatura de -10 grados Celsius, se necesitarían 41.800 julios de energía.
¿Qué ocurre cuando se añade más energía al líquido?
Cuando se añade más energía al líquido, aumenta la velocidad de las moléculas y la distancia entre ellas, lo que resulta en un aumento de la temperatura y a la eventual evaporación del agua. La evaporación es un cambio de estado de líquido a gas y ocurre cuando las moléculas de agua tienen suficiente energía para escapar de la superficie del líquido. La cantidad de energía necesaria para evaporar una cantidad determinada de agua se llama calor latente de vaporización y es de 40,7 kJ/mol para el agua.
¿Qué ocurre si se quita energía del líquido?
Si se quita energía del líquido, disminuye la velocidad de las moléculas y la distancia entre ellas, lo que resulta en un descenso de la temperatura y la eventual solidificación del agua. La solidificación es un cambio de estado de líquido a sólido y ocurre cuando las moléculas de agua empiezan a agruparse y a formar una estructura cristalina. La cantidad de energía que se necesita para solidificar una cantidad determinada de agua se llama calor latente de fusión y es de 6,01 kJ/mol para el agua.
¿Por qué el hielo flota en el agua?
El hielo flota en el agua porque es menos denso que el líquido. Cuando el agua se congela, las moléculas de agua se agrupan en una estructura cristalina, lo que resulta en una mayor separación entre las moléculas y por lo tanto, una disminución de la densidad. Por lo tanto, el hielo flota en el agua porque tiene una densidad menor que el líquido.
¿Por qué el agua se expande al congelarse?
El agua se expande al congelarse porque la estructura cristalina del hielo ocupa más espacio que las moléculas de agua en estado líquido. A medida que las moléculas de agua se agrupan en una estructura cristalina durante la solidificación, ocupan más espacio y por lo tanto, el volumen del agua aumenta. Este aumento de volumen puede ser perjudicial para los objetos que contienen agua y que se congelan, ya que puede causar daños estructurales.
Conclusión
El cambio de estado de un cubo de hielo de sólido a líquido es un proceso común que ocurre en nuestro día a día. Este cambio se produce cuando se añade suficiente energía para que las moléculas de agua empiecen a moverse libremente y rompan las uniones que las mantenían fijas en la estructura cristalina. La cantidad de energía necesaria para derretir un cubo de hielo depende de la masa del hielo y de la cantidad de calor que se le añada, y se puede calcular utilizando la ecuación Q = m x c x deltaT. Además, el hielo flota en el agua porque es menos denso que el líquido y el agua se expande al congelarse debido a la estructura cristalina del hielo.
Preguntas frecuentes
1. ¿Por qué el hielo se derrite más rápido en agua caliente que en agua fría?
El hielo se derrite más rápido en agua caliente que en agua fría porque el agua caliente tiene una temperatura mayor y por lo tanto, más energía. Esta energía se transfiere al hielo más rápidamente, lo que resulta en un aumento de la temperatura del hielo

Deja una respuesta