Que establece la ley de la conservacion de la masa
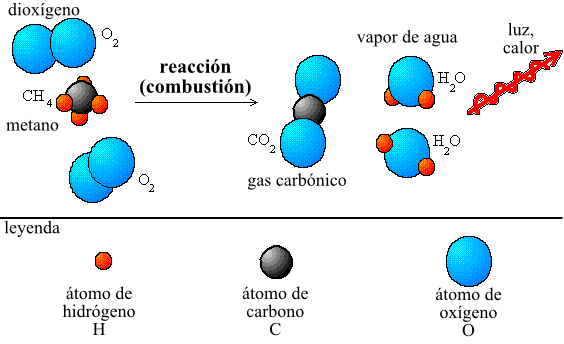
La ley de la conservación de la masa es uno de los principios fundamentales de la química. Esta ley establece que en cualquier reacción química, la masa total de los reactivos es igual a la masa total de los productos. En otras palabras, la masa no se crea ni se destruye, solo se transforma.
Esta ley fue propuesta por primera vez por el químico francés Antoine Lavoisier en el siglo XVIII. Lavoisier observó que la masa total de los reactivos y los productos de una reacción química siempre era la misma, sin importar las condiciones en las que se realizaba la reacción. A partir de estas observaciones, propuso la ley de la conservación de la masa.
La ley de la conservación de la masa es una consecuencia directa de la ley de la conservación de la energía. Esta última establece que la energía no se crea ni se destruye, solo se transforma. Como la masa y la energía están relacionadas por la famosa ecuación E=mc², la ley de la conservación de la masa es una consecuencia directa de la ley de la conservación de la energía.
La ley de la conservación de la masa se aplica a cualquier tipo de reacción química, ya sea una combustión, una reacción ácido-base o una reacción de precipitación. En todas estas reacciones, la masa total de los reactivos es igual a la masa total de los productos.
En la práctica, la ley de la conservación de la masa se utiliza para calcular la cantidad de reactivos necesarios para obtener una cierta cantidad de productos, o para determinar la cantidad de productos que se obtienen a partir de una cierta cantidad de reactivos. Por ejemplo, si se quema una cierta cantidad de gasolina en un motor de combustión interna, se puede calcular la cantidad de dióxido de carbono y agua que se producen a partir de la cantidad de gasolina utilizada.
La ley de la conservación de la masa también tiene importantes implicaciones teóricas. Por ejemplo, esta ley implica que la masa atómica de los elementos es constante, ya que la masa total de los reactivos y los productos siempre es la misma. Además, la ley de la conservación de la masa es una de las bases de la estequiometría, la rama de la química que estudia las relaciones cuantitativas entre los reactivos y los productos de una reacción química.
En resumen, La ley de la conservación de la masa establece que la masa total de los reactivos es igual a la masa total de los productos en cualquier reacción química. Esta ley tiene importantes implicaciones teóricas y prácticas en la química, y es una de las leyes más fundamentales de esta disciplina.
- ¿Cómo se aplica la ley de la conservación de la masa en la vida cotidiana?
- ¿Qué relación hay entre la ley de la conservación de la masa y la ley de la conservación de la energía?
- ¿Qué pasaría si la ley de la conservación de la masa no se cumpliera?
- ¿Cómo se puede demostrar experimentalmente la ley de la conservación de la masa?
- ¿Qué importancia tiene la ley de la conservación de la masa en la química?
¿Cómo se aplica la ley de la conservación de la masa en la vida cotidiana?
La ley de la conservación de la masa se aplica en muchos aspectos de la vida cotidiana. Por ejemplo, cuando se cocina una comida, la masa total de los ingredientes utilizados es igual a la masa total de la comida cocinada. Del mismo modo, cuando se quema una vela, la masa total de la cera y el oxígeno utilizados es igual a la masa total del dióxido de carbono y el agua producidos.
¿Qué relación hay entre la ley de la conservación de la masa y la ley de la conservación de la energía?
La ley de la conservación de la masa y la ley de la conservación de la energía están relacionadas por la famosa ecuación E=mc², propuesta por Albert Einstein. Esta ecuación establece que la masa y la energía están relacionadas, y que la masa puede convertirse en energía y viceversa. Por lo tanto, la ley de la conservación de la masa es una consecuencia directa de la ley de la conservación de la energía.
¿Qué pasaría si la ley de la conservación de la masa no se cumpliera?
Si la ley de la conservación de la masa no se cumpliera, significaría que la masa podría crearse o destruirse durante una reacción química. Esto violaría uno de los principios fundamentales de la física, y tendría importantes implicaciones teóricas y prácticas en la química y otras disciplinas científicas.
¿Cómo se puede demostrar experimentalmente la ley de la conservación de la masa?
La ley de la conservación de la masa se puede demostrar experimentalmente de varias maneras. Una de las formas más simples es pesar los reactivos antes de una reacción química, y luego pesar los productos después de la reacción. Si la masa total de los reactivos es igual a la masa total de los productos, se cumple la ley de la conservación de la masa.
¿Qué importancia tiene la ley de la conservación de la masa en la química?
La ley de la conservación de la masa es una de las leyes fundamentales de la química, y tiene importantes implicaciones teóricas y prácticas en esta disciplina. Esta ley se utiliza para calcular la cantidad de reactivos necesarios para obtener una cierta cantidad de productos, o para determinar la cantidad de productos que se obtienen a partir de una cierta cantidad de reactivos. Además, la ley de la conservación de la masa es una de las bases de la estequiometría, la rama de la química que estudia las relaciones cuantitativas entre los reactivos y los productos de una reacción química.

Deja una respuesta